Skyhawk Therapeutics ogłasza dziewięciomiesięczne wyniki pośrednie badań klinicznych fazy 1 nad lekiem SKY-0515 stosowanym w leczeniu choroby Huntingtona
10 hours ago
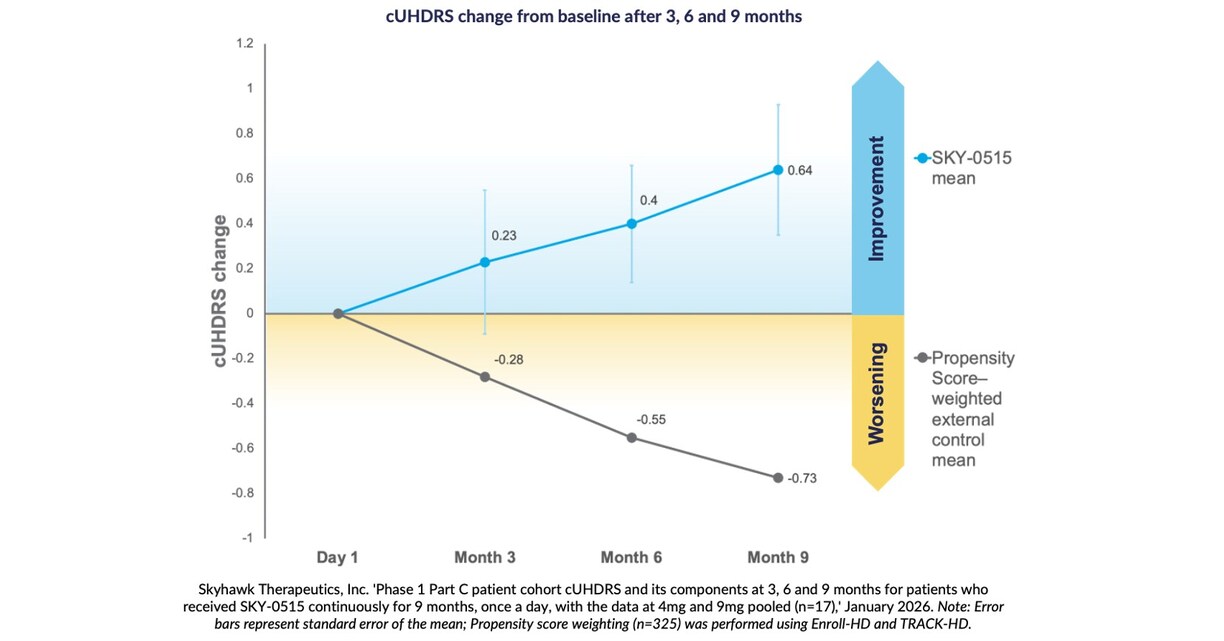
Wyniki z dziewięciu miesięcy pokazują średnią poprawę w Ujednoliconej Skali Oceny Choroby Huntingtona (Composite Unified Huntington's Disease Rating Scale, cUHDRS) o +0,64 punktu w stosunku do wartości wyjściowej, w porównaniu z przewidywanym pogorszeniem w naturalnym przebiegu choroby o -0,73 punktu u pacjentów z objawami w ciągu dziewięciu miesięcy, w oparciu o ważenie wykonane metodą odwrotności prawdopodobieństwa.
Skyhawk ogłasza również, że badania fazy 2/3 o nazwie FALCON-HD nad lekiem SKY-0515 zostało rozszerzone na cały świat. Skyhawk podał już lek ponad 90 pacjentom.
BOSTON, 27 stycznia 2026 r. /PRNewswire/ -- Skyhawk Therapeutics, Inc., firma biotechnologiczna zajmująca się badaniami klinicznymi, opracowująca nowatorskie terapie oparte na małych cząsteczkach w celu modulowania kluczowych celów RNA, ogłasza dzisiaj pozytywne wyniki dziewięciomiesięcznej analizy pośredniej dotyczącej badanego leku firmy na chorobę Huntingtona (HD) o nazwie SKY-0515.
Leczenie za pomocą SKY-0515 powoduje zależne od dawki zmniejszenie stężenia białka mHTT we krwi o 62% przy dawce 9 mg oraz zależne od dawki zmniejszenie stężenia mRNA PMS1 o 26%. PMS1 jest kluczowym czynnikiem powodującym somatyczną ekspansję powtórzeń CAG i patologię HD. Lek SKY-0515 wykazał również doskonałą ekspozycję w ośrodkowym układzie nerwowym i był ogólnie bezpieczny i dobrze tolerowany.
Po trzech, sześciu i dziewięciu miesiącach pacjenci otrzymujący SKY-0515 w kohorcie pacjentów części C badania klinicznego fazy 1 SKY-0515 wykazują średnią poprawę w Złożonej Ujednoliconej Skali Oceny Choroby Huntingtona (cUHDRS) w stosunku do wartości wyjściowej. Po dziewięciu miesiącach, w analizie zbiorczej, poprawa ta wynosiła +0,64 punktu w porównaniu z oczekiwanym pogorszeniem po dziewięciu miesiącach w skali cUHDRS u pacjentów z objawami wynoszącym -0,73 punktu, w oparciu o ważenie wykonane metodą odwrotności prawdopodobieństwa przy użyciu Enroll-HD i TRACK-HD.
„Dane dotyczące bezpieczeństwa i wstępnej skuteczności uzyskane w badaniach fazy 1 część C nad lekiem SKY-0515 u pacjentów dają duże nadzieje, ponieważ wykazują one odchylenie w skali cUHDRS od oczekiwanego pogorszenia stanu zdrowia w naturalnym przebiegu choroby po trzech, sześciu i dziewięciu miesiącach od rozpoczęcia badania, zgodnie z wcześniej ustalonym harmonogramem analiz - powiedział Ed Wild, profesor neurologii na University College London. - SKY-0515 nadal redukuje białko mHTT w największym stopniu spośród wszystkich dotychczas testowanych leków, a dane kliniczne i biomarkery wskazują, że lek jest dobrze tolerowany we wszystkich badanych dawkach. Zdolność SKY-0515 do redukcji zarówno mHTT, jak i PMS1 pozwala na skuteczne leczenie choroby Huntingtona poprzez oddziaływanie na dwa główne mechanizmy patogeniczne. Wyniki tych otwartych badań, które mają zostać zweryfikowane w trwającym badaniu FALCON-HD z grupą kontrolną otrzymującą placebo, dają nadzieję na znaczący wpływ na życie osób cierpiących na chorobę Huntingtona na całym świecie, dla których doustnie podawane leki obniżające poziom huntingtiny, takie jak SKY-0515, będą prawdziwą rewolucją".
„Naszym celem w badaniu fazy 1 było ustalenie bezpieczeństwa i aktywności biomarkerów - powiedział Sergey Paushkin, dyrektor ds. badań i rozwoju w Skyhawk Therapeutics - a utrzymująca się siła odpowiedzi biomarkerów SKY-0515 w naszej dziewięciomiesięcznej analizie danych pośrednich - i poprawa potencjalnego punktu końcowego, cUHDRS, w porównaniu z pogorszeniem wyniku cUHDRS w danych dotyczących naturalnego przebiegu choroby u pacjentów - podkreśla potencjał SKY-0515 jako najlepszej w swojej klasie terapii modyfikującej przebieg choroby Huntingtona. Te dane pośrednie stanowią ważny kamień milowy dla SKY-0515 i podkreślają zdolność platformy Skyhawk do dostarczania najlepszych w swojej klasie małych cząsteczek do leczenia wyniszczających chorób, dla których nie ma zatwierdzonych terapii modyfikujących przebieg choroby".
Choroba Huntingtona jest rzadką, dziedziczną i ostatecznie śmiertelną chorobą neurodegeneracyjną, która dotyka ponad 40 000 osób z objawami w Stanach Zjednoczonych, a szacuje się, że na całym świecie cierpi na nią setki tysięcy osób. Obecnie nie ma zatwierdzonych metod leczenia, które spowalniałyby lub zatrzymywały postęp choroby. SKY-0515 to doustny, badany modulator RNA o małej masie cząsteczkowej, opracowany w oparciu o nowatorską platformę modulującą RNA firmy SKYSTAR®. SKY-0515 terapeutycznie redukuje zarówno białko HTT, jak i białko PMS1. PMS1 jest dodatkowym kluczowym czynnikiem powodującym somatyczną ekspansję powtórzeń CAG i patologię HD i powinien uzupełniać korzyści płynące z redukcji zmutowanego HTT.
Firma Skyhawk poinformowała również dzisiaj, że badanie fazy 2/3 leku SKY-0515 o nazwie FALCON-HD l, prowadzone w dwunastu ośrodkach w Australii i Nowej Zelandii, zostało rozszerzone na cały świat. Jak dotąd lek SKY-0515 podano ponad 90 pacjentom.
SKY-0515 jest pierwszym lekiem Skyhawk objętym badaniami klinicznymi.
Do końca 2027 r. firma Skyhawk planuje wprowadzić do użytku klinicznego kolejne leki małocząsteczkowe przeznaczone do leczenia rzadkich chorób neurologicznych, dla których nie ma zatwierdzonych terapii modyfikujących przebieg choroby.
Badanie kliniczne fazy 1 dotyczące leku SKY-0515Badanie kliniczne fazy 1 dotyczące leku SKY-0515 to pierwsze badanie prowadzone na ludziach mające na celu ocenę bezpieczeństwa, tolerancji, farmakokinetyki i farmakodynamiki leku SKY-0515 u zdrowych ochotników i osób we wczesnym stadium choroby Huntingtona (HD). Badanie podzielono na trzy części. W częściach A i B oceniano SKY-0515 u zdrowych ochotników. Część C to badanie z podwójnie ślepą próbą, z grupą kontrolną otrzymującą placebo, prowadzone równolegle, w którym porównuje się dwa poziomy dawkowania leku SKY-0515 i placebo u osób we wczesnym stadium choroby Huntingtona (HD-ISS stadium 1, 2 lub łagodne stadium 3) przez 84 dni, a następnie przedłużone o 12 miesięcy aktywne leczenie, w którym wszyscy uczestnicy otrzymają niską lub wysoką dawkę SKY-0515 metodą ślepą. Cele badania obejmują ocenę zmutowanego białka HTT i mRNA PMS1. W części C badania SKY-0515 pierwsi pacjenci otrzymali dawkę leku w styczniu 2025 r. Nabór do badania fazy 1C SKY-0515 został zakończony.
Badanie kliniczne fazy 2/3 o nazwie FALCON-HD dotyczące leku SKY-0515FALCON-HD (NCT06873334) to randomizowane, podwójnie ślepe, kontrolowane placebo i obejmujące różne dawki badanie fazy 2/3 mające na celu ocenę farmakodynamiki, bezpieczeństwa i skuteczności leku SKY-0515 u 120 uczestników z chorobą Huntingtona w stadium 2 i wczesnym stadium 3 w 12 ośrodkach w Australii i Nowej Zelandii oraz u 400 uczestników z chorobą Huntingtona w stadium 2 i wczesnym stadium 3 w ponad 40 ośrodkach na całym świecie. Kwalifikujący się pacjenci będą otrzymywać raz dziennie doustną dawkę SKY-0515 w jednym z trzech poziomów dawkowania lub placebo przez okres leczenia trwający co najmniej 12 miesięcy. Badanie ma na celu ocenę potencjału leku SKY-0515 w modulowaniu splicingu RNA i redukcji białek mHTT i PMS1, które są związane z patologią choroby Huntingtona. Dodatkowe informacje na temat badania FALCON-HD, w tym listę ośrodków uczestniczących w badaniu i kryteria kwalifikacyjne, można znaleźć na stronach ClinicalTrials.gov i www.FALCON-HD.com.
Skyhawk TherapeuticsSkyhawk Therapeutics to firma biotechnologiczna zajmująca się badaniami klinicznymi, która wykorzystuje autorską platformę SKYSTAR® do odkrywania i opracowywania terapii opartych na małych cząsteczkach RNA, przeznaczonych do leczenia najtrudniejszych do wyleczenia chorób na świecie. Więcej informacji można znaleźć na stronie www.skyhawktx.com.
KONTAKTMaura McCarthydyrektor ds. rozwoju korporacyjnegoe-mail: [email protected]
Zdjęcie - https://mma.prnewswire.com/media/2870056/Skyhawk_Therapeutics_9_MONTH_DATA_Graph.jpgLogo - https://mma.prnewswire.com/media/710814/Skyhawk_Therapeutics_Logo.jpg
...Read the fullstory
It's better on the More. News app
✅ It’s fast
✅ It’s easy to use
✅ It’s free